L’intestin humain abrite près de 100 000 milliards de bactéries, un écosystème complexe qui influence notre santé bien au-delà de la simple digestion. Aujourd’hui, des scientifiques de Stanford franchissent une étape décisive en transformant certaines de ces bactéries en véritables usines pharmaceutiques vivantes, ouvrant la voie à une médecine personnalisée d’un genre totalement nouveau.
Quand les bactéries deviennent des alliées thérapeutiques
Le concept révolutionnaire développé par l’équipe de Stanford repose sur une idée audacieuse : plutôt que de combattre les bactéries intestinales, pourquoi ne pas les reprogrammer pour qu’elles produisent leurs propres médicaments directement dans notre corps ? Cette approche biomimétique exploite le fait que notre microbiome intestinal constitue déjà un laboratoire biochimique naturel d’une complexité inégalée.
Les chercheurs ont jeté leur dévolu sur Phocaeicola vulgatus, une bactérie déjà présente naturellement dans l’intestin humain. Leur objectif : la transformer en un destructeur d’oxalate, cette molécule responsable de la formation des redoutables calculs rénaux qui affectent des millions de personnes dans le monde.
Une ingénierie génétique sophistiquée
La modification génétique de Phocaeicola vulgatus relève d’un véritable tour de force biotechnologique. Les scientifiques ont introduit dans son génome la capacité de décomposer efficacement l’oxalate, tout en rendant la bactérie dépendante d’un nutriment spécifique : le porphyrane, dérivé des algues marines.
Cette dépendance nutritionnelle constitue un mécanisme de sécurité ingénieux. En contrôlant l’apport en porphyrane, les médecins peuvent moduler la population bactérienne : augmenter le nutriment pour stimuler la croissance des bactéries thérapeutiques, ou le réduire pour les éliminer progressivement de l’organisme. Ce système offre un contrôle précis sur le traitement, une caractéristique essentielle pour toute application médicale.
Des résultats prometteurs mais contrastés
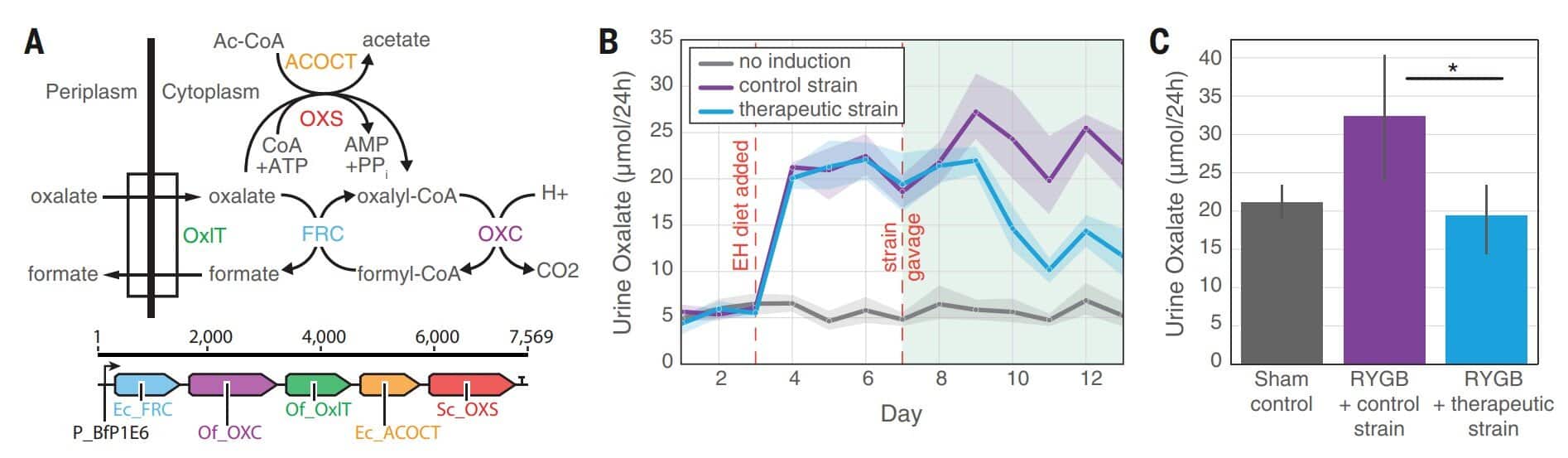
Les premiers tests sur des rats ont donné des résultats spectaculaires. Les animaux nourris avec un régime riche en oxalate ont vu leur concentration urinaire d’oxalate chuter de 47% après colonisation par les bactéries modifiées. Plus impressionnant encore, lors de simulations de chirurgie bariatrique – connue pour provoquer une hyperoxalurie chez l’humain – les bactéries thérapeutiques ont complètement neutralisé l’augmentation d’oxalate normalement observée.
L’essai clinique mené sur 39 volontaires sains, dont les détails sont rapportés dans la revue Science, a confirmé la faisabilité du concept chez l’humain. La colonisation s’est révélée dose-dépendante et généralement réversible, démontrant que le système de contrôle nutritionnel fonctionnait comme prévu. Cependant, deux participants ont conservé les bactéries modifiées même après arrêt du traitement, révélant une problématique inattendue.
Les défis de la mutation génétique
Cette persistance imprévisible cache un phénomène fascinant mais préoccupant : les bactéries modifiées peuvent échanger du matériel génétique avec leurs voisines intestinales, un processus naturel appelé transfert horizontal de gènes. Ces mutations peuvent altérer les propriétés thérapeutiques des bactéries ou leur conférer une indépendance vis-à-vis du système de contrôle nutritionnel.
Chez les patients atteints d’hyperoxalurie entérique – une pathologie caractérisée par une absorption excessive d’oxalate – les résultats se sont révélés plus mitigés. Six participants sur neuf ont montré une réduction moyenne de 27% des oxalates urinaires, un progrès encourageant mais statistiquement non significatif en raison de la taille réduite de l’échantillon.
Une fenêtre sur l’avenir de la médecine
Au-delà du traitement spécifique des calculs rénaux, cette recherche ouvre des perspectives révolutionnaires pour la médecine du futur. Le principe de transformer notre propre microbiome en pharmacie personnalisée pourrait s’appliquer à une multitude de pathologies : troubles métaboliques, maladies inflammatoires, déficiences enzymatiques, ou même certains cancers.
L’avantage conceptuel est considérable : plutôt que d’administrer des médicaments externes nécessitant des doses répétées, le traitement se déploie en continu, directement là où il est nécessaire, avec une précision biologique naturelle. Cette approche pourrait réduire les effets secondaires systémiques tout en maximisant l’efficacité thérapeutique.
Les prochaines étapes du développement
Malgré les défis identifiés, les chercheurs de Stanford restent optimistes. Leur étude prouve qu’une colonisation contrôlée et prolongée avec des bactéries génétiquement modifiées reste possible et sûre chez l’humain. Les recherches futures se concentreront sur l’amélioration des mécanismes de contrôle et la réduction des risques de mutations non désirées.
Cette avancée marque potentiellement le début d’une ère nouvelle où nos propres bactéries intestinales deviendraient nos partenaires thérapeutiques les plus intimes, transformant radicalement notre approche du traitement médical et ouvrant la voie à une médecine véritablement personnalisée.